No products in the cart.

A Anvisa publicou a Resolução – RDC nº 843, de 22 de fevereiro de 2024 que dispõe sobre a regularização de alimentos e embalagens sob competência do Sistema Nacional de Vigilância Sanitária (SNVS) destinados à oferta no território nacional.
A norma é complementada pela Instrução Normativa – IN nº 281, de 22 de fevereiro de 2024 que estabelece a forma de regularização das diferentes categorias de alimentos e embalagens, e a respectiva documentação que deve ser apresentada.
Em primeira mão, preparei um texto abrangente para auxiliar na compreensão e no início dos preparativos para as modificações necessárias.😁🙌
Contextualização
Ambas as normas são resultados de Consultas Públicas realizadas em 2022 e estabelecem o marco regulatório para registro, notificação e comunicação de início de fabricação ou importação de alimentos e embalagens. Após 24 anos, essas normas revogam a RDC nº 22 e 23 de 2000.😯
O processo de revisão das Resoluções nº 22 e 23/2000 teve início em 2007, ganhando formalidade e velocidade a partir de 2009, com a abertura das Consultas Públicas nº 95/2009 e nº 52/2011, esta última consolidada em 2012 pela Diretoria Colegiada (Dicol) da Anvisa. A proposta aprovada incluía condições, destacando o Sistema de Peticionamento Eletrônico de Notificação de Alimentos como um dos principais pontos.
Entretanto, após a disponibilização do sistema para testes, alguns pontos foram considerados críticos, impedindo a conclusão do procedimento de regularização. Em 2013, a DICOL decidiu, por maioria, revogar a decisão anterior de aprovação, sugerindo uma avaliação das implicações e a não publicação do texto.
Em 2014, a Lei nº 13.001 isentou agricultores familiares, microempreendedores individuais e empreendedores da economia solidária da taxa de fiscalização sanitária, atendendo a preocupações registradas em reuniões da DICOL de 2012 e 2013.
No mesmo ano, a GGALI reavaliou a proposta, resultando na divisão do texto original em duas partes: uma minuta de RDC com disposições gerais sobre notificação e registro e uma minuta de Instrução Normativa (IN) com procedimentos específicos para regularização de produtos.
Em 2016, a GGALI iniciou uma segunda fase de discussões das regras de regularização, dentro de uma nova estrutura organizacional mais especializada.
Em 2018, oficinas foram organizadas para mapear problemas regulatórios, e em 2019, com a publicação da Lei nº 13.874, foi necessário uma readequação para continuar a revisão das normas de regularização de alimentos, principalmente sobre os critérios de riscos.
Em 2019, uma decisão judicial levou à criação da categoria “Água do mar dessalinizada potável e envasada,” sujeita a registro obrigatório conforme a RDC nº 316/2019, resultando em uma matriz de decisão com categorias de regularização.
A RDC nº 460/2020, publicada em 2020, adicionou as Fórmulas dietoterápicas para erros inatos do metabolismo às categorias de regularização de alimentos, exigindo uma revisão do tema.
Em 2021, o tema foi incluído na AR 2021-2023, projeto 3.8 – Modernização do marco regulatório, fluxos e procedimentos para a regularização de alimentos, posteriormente migrando para AR 2024-2025, Tema 3.22 – Revisão da regulamentação sobre a regularização de alimentos dispensados de registro.
Em 2022, foi aberto o processo regulatório para estabelecer os procedimentos para a regularização de alimentos e embalagens sob a competência do Sistema Nacional de Vigilância Sanitária (SNVS). Em 08/09/2022, foram publicadas as Consultas Públicas nº 1113 e 1114, com um prazo de contribuição de 90 dias.
Os resultados das consultas públicas podem ser visualizados abaixo:
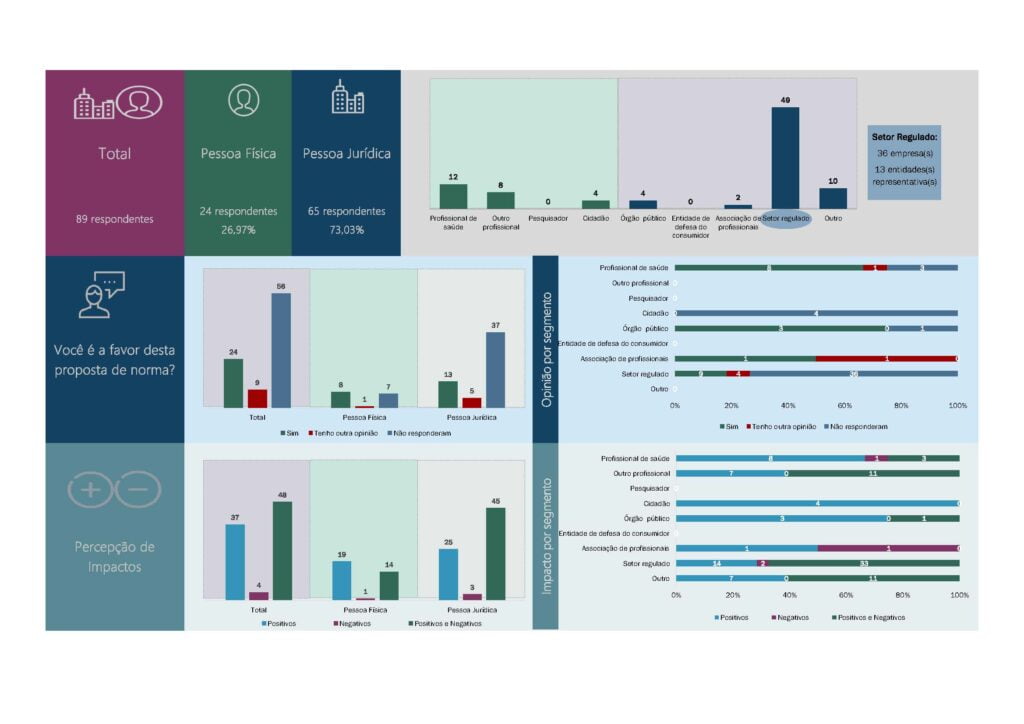
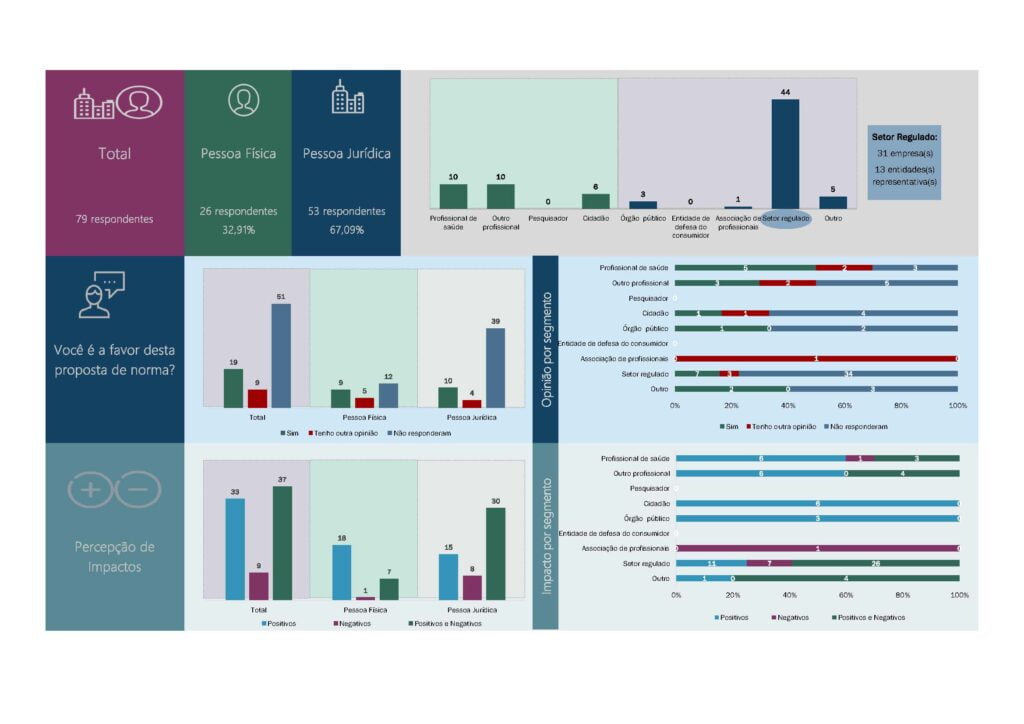
Finalmente, em 21 de fevereiro de 2024, o tema foi votado na 1ª Reunião ordinária da DICOL (assista aqui), e na data de hoje, 28 de fevereiro de 2024 (meu aniversário 😊), temos a publicação das normas!
Estrutura das normas
A Resolução – RDC nº 843, de 22 de fevereiro de 2024, é composta por 6 capítulos e 41 artigos, distribuídos da seguinte forma:
- Capítulo I – Disposições preliminares
- Capítulo II – Requisitos gerais para a regularização de alimentos e embalagens
- Capítulo III – Requisitos específicos para registro, revalidação, cancelamento e alterações pós-registros
- Capítulo IV – Requisitos específicos para notificação e avaliação, manutenção, cancelamento e alterações da notificação
- Capítulo V – Comunicado de início de fabricação ou importação e alteração e cancelamento do comunicado
- Capítulo VI – Disposições finais e transitórias
Por sua vez, a Instrução Normativa – IN nº 281, de 22 de fevereiro de 2024, estabelece a forma de regularização das diferentes categorias por meio de 11 anexos:
- Anexo I define as categorias de alimentos e embalagens sujeitas à obrigatoriedade de registro junto à Anvisa.
- Anexo II define as categorias de alimentos e embalagens sujeitas à obrigatoriedade de notificação junto à Anvisa.
- Anexo III define as categorias de alimentos e embalagens sujeitas à obrigatoriedade de comunicação de início de fabricação ou importação junto à autoridade sanitária do Estado, do Distrito Federal ou do Município.
- Anexo IV define as categorias de alimentos e embalagens que não estão sujeitas à regularização junto ao Sistema Nacional de Vigilância Sanitária (SNVS).
- Anexo V estabelece os documentos gerais necessários para a instrução das solicitações de registro.
- Anexo VI estabelece os documentos complementares necessários para a instrução das solicitações de registro, por categoria de produto.
- Anexo VII estabelece os documentos necessários para a instrução das solicitações de revalidação de registro.
- Anexo VIII define os tipos de alterações pós-registro, sua finalidade, condição de implementação e os documentos necessários para a instrução das solicitações de alterações pós-registro.
- Anexo IX define o documento que deve ser apresentado com as justificativas para a realização das alterações pós-registro.
- Anexo X estabelece os documentos necessários para a instrução das notificações, conforme a categoria do produto.
- Anexo XI estabelece o formulário com as informações obrigatórias que devem constar no comunicado de início de fabricação ou importação do produto.
Entendendo as novas regras
A RDC nº 843/2024 abrange os procedimentos relacionados a:
I – registro, alterações pós-registro, revalidação de registro e cancelamento de registro (conforme Anexo I da IN nº 281/2024);
II – notificação, alteração de notificação, manutenção de notificação e cancelamento de notificação (conforme Anexo II da IN nº 281/2024); e
III – comunicado de início de fabricação ou importação, alteração do comunicado e cancelamento do comunicado (conforme Anexo III da IN nº 281/2024).
Os alimentos listados no Anexo IV da IN nº 281/2024 estão isentos dos requisitos de regularização e incluem:
- Matérias-primas alimentares;
- Alimentos in natura;
- Equipamentos para alimentos, inclusive os de uso doméstico;
- Produtos alimentícios e ingredientes, incluindo aditivos alimentares e coadjuvantes de tecnologia, elaborados de acordo com normas que estabelecem seus requisitos de composição, qualidade, segurança e rotulagem, sendo utilizados exclusivamente na produção de alimentos industrializados; e
- Produtos alimentícios manipulados e preparados em serviços de alimentação destinados à venda direta ao consumidor, como produtos de panificação, de pastifício, de pastelaria, de confeitaria, de doceria, de rotisseria, de sorveteria, de bares, de restaurantes, de cantinas, de unidades de alimentação e nutrição de serviços de saúde, de escolas, de creches, entre outros.
A regularização dos alimentos obrigatórios para registro (Anexo I da IN nº 281/2024) deve ser conduzida pela matriz do fabricante, representante do fabricante ou importador. Para a categoria dos alimentos e embalagens com obrigatoriedade de notificação (Anexo II da IN nº 281/2024), o processo também deve ser realizado por essas entidades.
No caso da categoria dos alimentos com obrigatoriedade de comunicação do início de fabricação ou importação (Anexo III da IN nº 281/2024), a regularização é de responsabilidade do fabricante ou importador.
Responsabilidades
A detentora da regularização é responsável, conforme o Art. 5º da RDC nº 843/2024, por:
I – Garantir a veracidade, correção e atualização das informações apresentadas nos procedimentos de regularização;
II – Responder pela garantia dos requisitos sanitários de composição, qualidade, segurança e rotulagem estabelecidos para o produto regularizado;
III – Solicitar alteração das informações prestadas no processo de regularização sempre que o produto sofrer modificação por sua iniciativa, do fabricante, por atualização da legislação ou por determinação da autoridade sanitária;
IV – Solicitar revalidação de registro ou manutenção da notificação sempre que houver interesse na continuidade de disponibilização do produto no mercado; e
V – Solicitar o cancelamento da regularização quando não houver mais interesse na oferta do produto.
Para os produtos categorizados no Anexo I e II da IN nº 281/2024, a detentora deve:
I – Realizar o cadastro no sistema da Anvisa e mantê-lo atualizado; e
II – Informar, no momento da solicitação de regularização, todos os fabricantes do produto que realizam atividades de produção, controle de qualidade e armazenamento, indicando suas respectivas responsabilidades.
É importante ressaltar que todos os fabricantes responsáveis por atividades de produção, controle de qualidade e armazenamento dos produtos devem estar cadastrados no sistema da Anvisa, sendo responsáveis por manter atualizadas todas as informações declaradas.
Requisitos para registro e revalidação, cancelamento e alterações pós-registros
As solicitações de registro devem ser protocoladas na Anvisa por meio de petição com um código de assunto específico para a categoria do produto, conforme os documentos descritos nos Anexos V e VI da IN nº 281/2024.
O produto registrado permanece inalterado, com o registro concedido por meio de publicação no Diário Oficial da União (DOU), e a oferta do produto só pode ser iniciada após essa publicação. Alimentos registrados devem conter a declaração “Alimento registrado na Anvisa:”, seguida do número completo do registro publicado no DOU. O prazo de validade é de 5 anos a partir da data de publicação.
Revalidações dos registros devem ser protocoladas por meio de petição com código de assunto específico para a categoria do produto, com antecedência máxima de 12 meses e mínima de 3 meses do vencimento do registro. Isso deve seguir os documentos descritos no Anexo VII da IN nº 281/2024.
O cancelamento do registro do produto pode ocorrer quando a detentora solicitar seu cancelamento, quando a petição de revalidação de registro for indeferida ou quando não solicitar ou solicitar fora do prazo a revalidação do registro. O cancelamento será publicado no DOU.
Em caso de indeferimento da revalidação do registro, o cancelamento ocorrerá somente após o vencimento e a manutenção da decisão de indeferimento pelas instâncias administrativas recursais. Se a revalidação não for solicitada ou for solicitada fora do prazo, o cancelamento ocorrerá somente após o vencimento por caducidade.
Alterações pós-registros também devem ser apresentadas por meio de petição com código de assunto específico para cada tipo de alteração, seguindo os documentos descritos nos Anexos VIII e IX da IN nº 281/2024.
Requisitos para notificação e avaliação, manutenção, cancelamento e alterações da notificação.
A grande novidade são os procedimentos para notificação, avaliação, manutenção, cancelamento e alterações de notificações de produtos abrangidos no Anexo II da IN nº 281/2024.
Os produtos que necessitam de notificação são:
- Água do mar dessalinizada, potável e envasada
- Alimentos com alegações de propriedade funcional e/ou de saúde
- Alimentos de transição para alimentação infantil
- Alimentos para controle de peso
- Cereais para alimentação infantil
- Resina de PET-PCR grau alimentício
- Artigo precursor ou embalagem final de PET-PCR grau alimentício
- Suplementos alimentares
A notificação deve ser protocolada junto à Anvisa por meio de petição com código de assuntos específico para a categoria do produto, devidamente instruída com os documentos descritos no Anexo X da IN nº 281/2024. Se os produtos possuírem mais de uma apresentação, a petição deve conter informações sobre todas as apresentações. É importante destacar que a notificação que atenda aos requisitos da norma ocorrerá automaticamente, sem necessidade de avaliação prévia pela Anvisa.
Ressalta-se que a comercialização dos produtos só pode ser iniciada após o protocolo da notificação. Na rotulagem desses produtos, deve constar a informação “Alimento notificado na Anvisa”, seguida do número completo do processo de notificação.
Avaliação da Notificação
A avaliação da notificação pode ser realizada a qualquer momento pela Anvisa, que também pode requerer informações adicionais além daquelas protocoladas na notificação.
Caso incorreções sejam identificadas, a Anvisa poderá:
I – Notificar a detentora sobre as correções necessárias na notificação do produto, indicando o prazo para adequação;
II – Realizar as correções e notificar a detentora sobre as adaptações a serem implementadas no produto, indicando o prazo de adequação; ou
III – Cancelar a notificação do produto e notificar a detentora sobre as medidas a serem adotadas, caso as incorreções representem risco à saúde do consumidor.
Os protocolos de notificação também estão sujeitos a manutenção a cada 5 anos. As empresas que não manifestarem interesse terão suas notificações inativadas. No entanto, mesmo após a inativação, a detentora pode protocolar, a qualquer momento, a solicitação de reativação por meio de petição individual para cada produto.
O cancelamento da notificação pode ocorrer quando a detentora solicitar o cancelamento ou quando forem identificadas incorreções que possam representar risco à saúde do consumidor.
Comunicado de Início de Fabricação ou importação e alteração e cancelamento do comunicado
O comunicado de início de fabricação ou importação aplica-se aos alimentos listados no Anexo III, por meio do protocolo do formulário do Anexo XI da IN nº 281/2024.
Todo produto só poderá ser comercializado após o devido protocolo do comunicado, sem que isso signifique que o produto foi “aprovado” pela autoridade sanitária.
A comunicação do início de fabricação tem validade indeterminada, e após a comunicação, a autoridade sanitária pode realizar inspeções nas unidades fabricantes ou armazenadoras dos alimentos ou embalagens.
Após a realização de uma comunicação de início de fabricação, ela pode ser alterada por meio de uma solicitação de alteração, resultando no cancelamento automático do comunicado inicial. Consequentemente, o produto alterado só pode ser disponibilizado após o novo protocolo.
Mesmo sendo um comunicado de início de fabricação ou importação, a detentora pode solicitar o cancelamento quando não houver mais interesse na oferta do produto, conforme estabelece o inciso V do Art. 5º da RDC nº 843/2024.
Prazo de adequações
Produtos com registro obrigatório
As empresas que possuem produtos enquadrados no Anexo I da IN nº 281/2024 e que estejam registrados até a data de 01/09/2024 terão um prazo de 2 anos, ou seja, até o dia 1º de setembro de 2026, para efetuarem as modificações nos alimentos com obrigatoriedade de registro (conforme Art. 30 da RDC nº 843/2023).
Para os mesmos produtos com vencimento até 01/09/2026, a revalidação pode ser solicitada no prazo de 60 dias antes da data de seu vencimento. Produtos fabricados até a data de publicação da decisão final sobre a solicitação de adequação podem ser disponibilizados no mercado até o final de seus prazos de validade.
É importante destacar que essas modificações devem ser realizadas mediante protocolo de petição específica de pós-registro, e o não cumprimento do prazo estabelecido resultará no cancelamento do registro.
Fórmulas dietoterápicas para erros inatos do metabolismo
As Fórmulas dietoterápicas para erros inatos do metabolismo passam a ter registro obrigatório, conforme estabelecido no Anexo I da IN nº 281/2024, e aquelas que tenham sido objeto de comunicação de início de fabricação ou importação terão até o dia 1º de setembro de 2025 para solicitar o registro junto à autoridade sanitária, conforme previsto no Art. 31 da RDC nº 843/2024.
Para esses produtos fabricados até a data de publicação da decisão final sobre a solicitação de registro, é permitida a sua disponibilização no mercado até o término de seus prazos de validade.
Alimentos para controle de peso e dos Suplementos Alimentares
Conforme as novas regras, os alimentos para controle de peso e os suplementos alimentares passam a ter notificação obrigatória, de acordo com o Anexo II da IN nº 281/2024. Aqueles que tenham sido objeto de comunicado de início de fabricação ou importação terão até o dia 1º de setembro de 2025 para realizar a notificação junto à autoridade sanitária, conforme estabelecido pelo Art. 32 da RDC nº 843/2024.
Esses produtos, fabricados até a data de notificação, podem ser disponibilizados no mercado até o término de seus prazos de validade.
Produtos que tinham registro obrigatório e passam a ter notificação obrigatória
Para os seguintes produtos:
I – água do mar dessalinizada, potável e envasada;
II – alimentos com alegações de propriedade funcional ou de saúde;
III – alimentos de transição para alimentação infantil;
IV – cereais para alimentação infantil;
V – resina, artigo precursor ou embalagem final de PET-PCR grau alimentício; e
VI – suplementos alimentares contendo probióticos ou enzimas.
Temos as seguintes condições:
- a) A notificação dos produtos que tenham sido registrados até a data de entrada em vigor da RDC nº 843/2024, ou seja, até o dia 01/09/2024, deve ser protocolada até o vencimento do seu registro;
- b) A notificação deve ser concomitante à solicitação de cancelamento de registro;
- c) Os produtos fabricados durante a vigência do registro podem ser disponibilizados no mercado até o final de seus prazos de validade;
- d) Não serão passíveis de alterações de pós-registros; e
- e) Não serão revalidados após a entrada em vigor desta Resolução.
Revogações e Alterações
Alteram-se as seguintes disposições:
I – O item 4.3 do Anexo da Portaria SVS/MS nº 27, de 18 de março de 1996;
II – Os itens 3.3, 3.5, 3.6, 3.7, 3.8 e 3.9 do Anexo da Resolução da Diretoria Colegiada – RDC nº 20, de 26 de março de 2008;
III – Art. 21 da Resolução da Diretoria Colegiada – RDC nº 243, de 26 de julho de 2018;
IV – Arts. 5º e 6º da Resolução da Diretoria Colegiada – RDC nº 241, de 26 de julho de 2018; e
V – Incluem-se os itens 3.6, 3.7 e 3,8 a Resolução – RES nº 18, de 30 de abril de 1999;
Revogam-se as seguintes disposições:
I – Resolução – RES nº 19, de 30 de abril de 1999;
II – Resolução da Diretoria Colegiada – RDC nº 22, de 15 de março de 2000;
III – Resolução da Diretoria Colegiada – RDC nº 23, de 15 de março de 2000;
IV – Resolução da Diretoria Colegiada – RDC nº 27, de 6 de agosto de 2010;
V – Resolução da Diretoria Colegiada – RDC nº 240, de 26 de julho de 2018;
VI – o item 10 do Anexo da Portaria SVS/MS n º 34, de 13 de janeiro de 1998;
VII – o item 10 do Anexo da Portaria SVS/MS n º 36, de 13 de janeiro de 1998;
VIII – os itens 10, 11 e 12 do Anexo da Resolução – RES nº 105, de 19 de maio de 1999;
X – o art. 23 e o Anexo I da Resolução da Diretoria Colegiada – RDC nº 460, de 21 de dezembro de 2020; e
XI – o art. 12 e o Anexo III da Resolução da Diretoria Colegiada – RDC nº 818, de 28 de setembro de 2023.
Vigência
As normas, RDC nº 843/2024 e IN nº 281/2024, entram em vigor no dia 1º de setembro de 2024.







